在免疫学的浩瀚星空中,巨噬细胞无疑是最具“百变气质”的明星。它们既是机体防御的“卫士”,又是组织修复的“工匠”。这种多面手的特性,源于它们惊人的可塑性——能够根据微环境的不同信号,分化成截然不同的表型。
今天,我们就来深度拆解巨噬细胞研究的“基本功”:如何在体外诱导巨噬细胞完成从M0(静息态)到M1(促炎型)或M2(抗炎型)的华丽转身。无论你是刚进实验室的小白,还是正在优化条件的科研老手,这份指南都将助你一臂之力。
认识你的“主角”:巨噬细胞的三重人格在动手实验之前,我们需要先搞清楚这三种状态的本质区别,这决定了我们后续诱导策略的制定。
M0型:待命的“白纸”M0型巨噬细胞是未极化的静息状态。它们就像是一张白纸,或者一个处于待命状态的士兵,具备基本的吞噬功能,但尚未被特定的信号激活去执行极端的杀伤或修复任务。在体外实验中,我们通常先获得M0细胞,作为后续极化的起点。
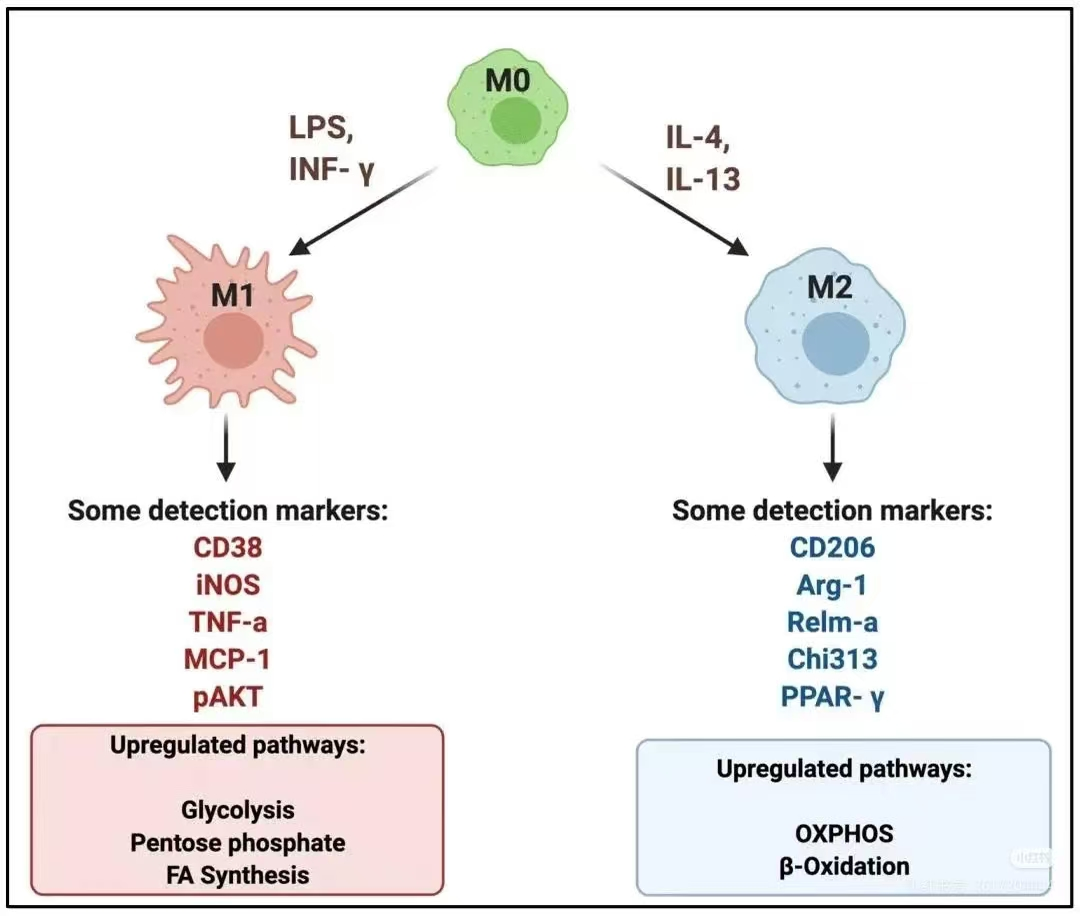
M1型:愤怒的“杀手”M1型巨噬细胞被称为“经典激活型”。当机体遭遇细菌、病毒入侵或发生炎症时,M1细胞会被迅速激活。它们性格火爆,高表达促炎因子(如TNF-α, IL-6, IL-1β),产生大量活性氧(ROS)和一氧化氮(NO),主要任务是杀伤病原体、清除肿瘤细胞,并引发强烈的炎症反应。
M2型:温柔的“修补匠”M2型巨噬细胞被称为“替代激活型”。当炎症消退或组织受损时,它们登场。M2细胞性格温和,高表达抗炎因子(如IL-10, TGF-β)和精氨酸酶-1(Arg-1)。它们的主要任务是抑制过度炎症、促进血管生成、修复受损组织以及清除细胞碎片。但在肿瘤微环境中,M2型往往被肿瘤细胞“策反”,成为帮凶。
选对“演员”:常见的细胞模型体外诱导巨噬细胞,主要依赖三种模型,它们的诱导策略略有不同:
THP-1细胞(人源单核细胞白血病细胞)这是最常用的人源细胞系。它们是悬浮生长的,必须先使用佛波酯(PMA)诱导分化为贴壁的M0巨噬细胞,才能进行后续的M1/M2极化。
BMDM(小鼠骨髓来源巨噬细胞)这是原代细胞,通过提取小鼠骨髓细胞,在M-CSF(巨噬细胞集落刺激因子)的作用下培养7天左右获得。BMDM更接近体内真实情况,但提取过程繁琐,且个体差异较大。
RAW264.7细胞(小鼠单核巨噬细胞白血病细胞)这是一种永生化细胞系,本身就具备一定的巨噬细胞特性。虽然可以直接刺激,但为了获得更好的效果,通常也建议先使其静息或低血清培养。
核心实操:诱导条件的“配方”这是大家最关心的部分。不同的细胞类型,所需的“变身药水”浓度和时间有所不同。以下是基于主流文献和实验经验的“黄金配方”。
第一阶段:获取M0(静息态)对于THP-1细胞:
关键试剂:PMA(佛波酯)。
常用浓度:50-100 ng/mL(也有文献使用低浓度25ng/mL长时间诱导以减少细胞损伤)。
诱导时间:24-48小时。
操作要点:加入PMA后,悬浮的THP-1细胞会逐渐贴壁,形态变不规则,出现伪足。诱导完成后,必须更换为不含PMA的新鲜培养基,静置培养24小时(Resting),让细胞恢复稳态,成为标准的M0。
对于BMDM:
关键试剂:M-CSF。
常用浓度:20-50 ng/mL。
诱导时间:6-7天。
操作要点:每3天半量换液,补充新鲜M-CSF。第7天获得的贴壁细胞即为M0。
第二阶段:向M1极化(黑化/战斗模式)一旦获得M0细胞,M1的诱导相对简单直接。
关键试剂:LPS(脂多糖)+ IFN-γ(干扰素-γ)。
LPS浓度:100 ng/mL(部分细胞系如RAW264.7对LPS极敏感,浓度可调整)。
IFN-γ浓度:20 ng/mL。
诱导时间:24-48小时。
鉴定标志:流式检测CD80、CD86高表达;qPCR检测iNOS、TNF-α、IL-1β、IL-6显著升高。
第三阶段:向M2极化(洗白/修复模式)M2的诱导通常需要更长的时间,且细胞因子较为昂贵。
关键试剂:IL-4 + IL-13。
IL-4浓度:20 ng/mL。
IL-13浓度:20 ng/mL。
诱导时间:48-72小时(M2极化通常比M1慢,建议培养48小时以上)。
鉴定标志:流式检测CD206(甘露糖受体)、CD163高表达;qPCR检测Arg-1、YM1(小鼠)、Fizz1显著升高。
避坑指南:实验失败的“罪魁祸首”很多同学在操作中会发现诱导效率极低,或者细胞状态极差。以下是几个最常见的“坑”:
PMA的毒性问题PMA虽然能诱导分化,但对细胞有毒性。浓度过高或作用时间过长会导致细胞死亡或过度激活,产生“假阳性”的炎症反应。
对策:尝试使用低浓度PMA(如25-50 ng/mL)诱导48小时,然后彻底洗去PMA,静置24小时后再进行极化。
细胞密度是关键巨噬细胞是群居动物,密度过低很难诱导成功,密度过高则容易营养耗竭。
对策:THP-1诱导时,建议密度控制在5×10^5 cells/mL左右。
细胞因子的活性LPS、IFN-γ、IL-4等因子非常娇贵,反复冻融极易失活。
对策:购买小包装,分装冻存,避免反复冻融。LPS溶解后通常4度保存短期使用,蛋白类因子建议-80度保存。
洗涤不彻底在THP-1从M0向M1/M2转变前,如果残留了PMA,可能会干扰极化效果。
对策:在加入极化因子前,用PBS轻柔洗涤细胞1-2次,并更换新鲜完全培养基。
种属差异小鼠和人的巨噬细胞对因子的反应不同。例如,小鼠M2诱导有时单用IL-4即可,而人源细胞通常建议IL-4+IL-13联用效果更佳。
结果验证:如何证明你成功了?做完实验只是第一步,拿出过硬的数据才是关键。
形态学观察(初筛)M1型:细胞通常变圆,折光性强,伪足较短或呈棘状,看起来“张牙舞爪”。
M2型:细胞通常呈长梭形或纺锤形,伪足较长,排列比较紧密。
注意:形态学仅供参考,不能作为唯一证据。
分子水平检测(金标准)qPCR:检测mRNA水平。M1看iNOS、TNF-α;M2看Arg-1、CD206。注意:iNOS和Arg-1是经典的互斥指标。
流式细胞术:检测表面标志物。M1看CD80/CD86;M2看CD206/CD163。
ELISA/Western Blot:检测上清液中的细胞因子分泌量(如IL-6 vs IL-10)或胞内蛋白表达。
结语巨噬细胞的极化研究,本质上是在模拟体内复杂的免疫微环境。虽然体外诱导模型无法完全复刻体内的复杂性,但它为我们理解免疫机制、筛选抗炎或抗肿瘤药物提供了最基础也最重要的窗口。
掌握M0、M1、M2的诱导秘籍,不仅仅是学会加几个因子,更是要理解细胞在不同信号刺激下的命运抉择。希望这份攻略能成为你实验台上的得力助手,助你早日获得漂亮的实验数据!
图片来源:小红书
